Scientific Reports | 模拟多专家会诊, 透彻未来破解泛癌冰冻诊断瓶颈
近日,中日友好医院联合透彻实验室的合作研究成果「Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision」于Scientific Reports发表。这项研究提出了一种基于软专家混合机制的弱监督视觉Transformer(Soft MoE-ViT)模型,术中冰冻切片病理诊断从传统的人工经验模式迈向了泛癌种、高精度、低成本的多专家决策体系。

术中冰冻切片病理诊断是指导手术范围、评估肿瘤良恶性与切缘状态的“术中金标准”,但切片质量易受组织折叠、冰晶、挤压、染色不均等影响,术中时间紧迫,对病理医师诊断水平要求极高。更具考验的是,微小肿瘤病灶易被炎症、纤维化掩盖,反应性不典型性增生易对诊断造成干扰。此外,传统深度学习模型对高性能算力的依赖导致了高昂的落地成本,也成为先进技术部署于医疗机构的隐形壁垒。因此,临床亟需一种既能敏锐识别形态细节,又能兼顾低成本、高效率的数智化工具,为术中诊断提供更稳固的诊断防线。
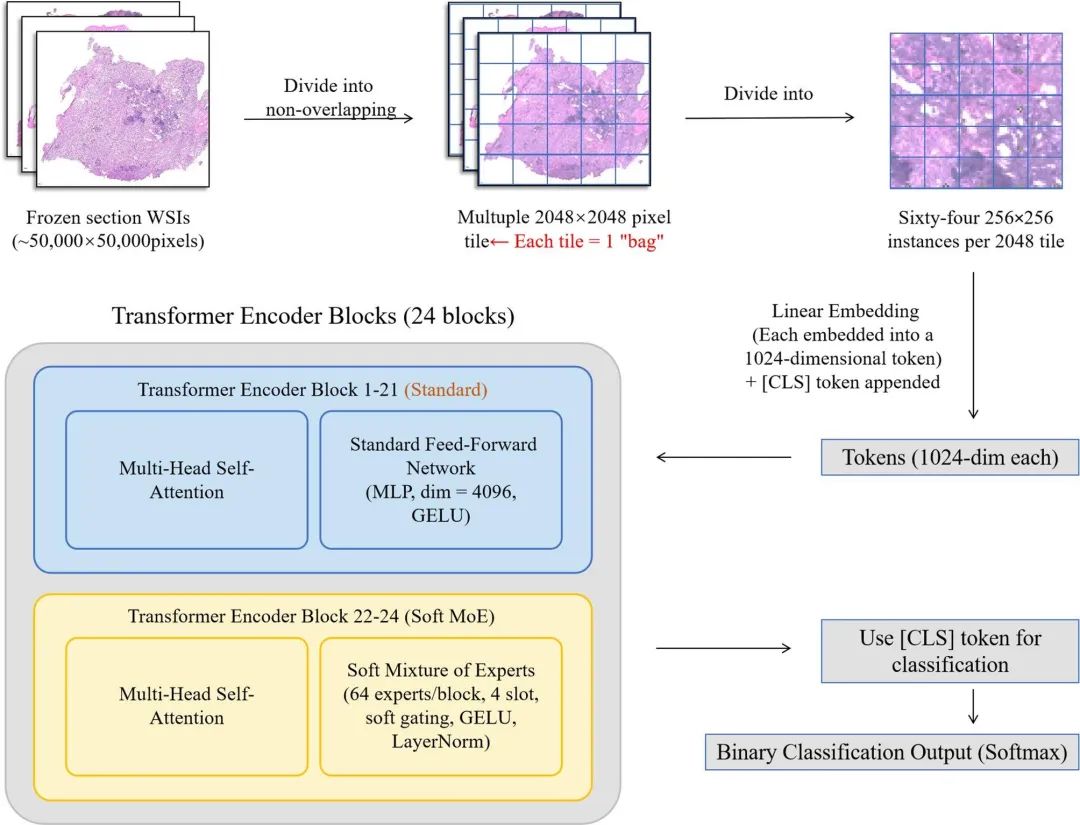
针对这一挑战,透彻未来联合中日友好医院构建了一个包含4,667张真实世界H&E染色术中冰冻全像素切片的大规模数据集,涵盖了肺部、乳腺、甲状腺、宫颈、淋巴结等多个部位肿瘤。与传统依赖像素级标注的模型不同,该研究在切片级标签的弱监督环境下,利用Soft MoE-ViT架构模拟了类似于多学科专家会诊的决策逻辑,通过软路由机制让多个并行专家网络能够加权处理复杂的图像特征,从而在存在冰晶、组织折叠等干扰的冰冻切片真实场景下实现了极高的诊断稳定性。实验结果显示,该模型在独立测试集中实现了0.957的AUC、90.4%的准确率以及96.1%的特异性,展现出卓越的判别能力。特别是在乳腺和肺组织标本中,模型的诊断敏感度均达到了100%,这证明其模型能够精准捕获跨器官通用的恶性组织病理学特征。
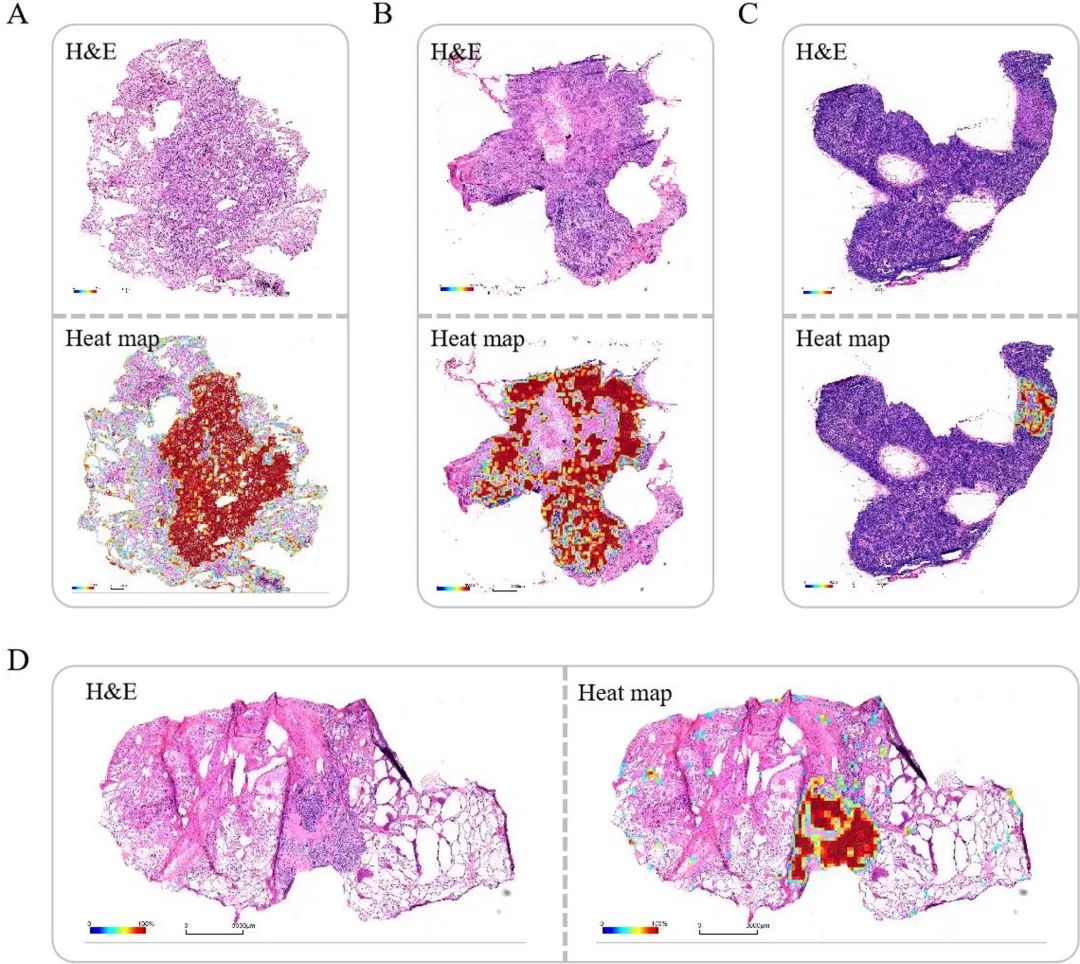
除了在诊断精度上实现了突破,模型能够像经验丰富的专家一样,通过热力图在复杂的组织背景中精准定位病变位置,极大增强了模型在实际应用中的临床可解释性。经资深病理专家独立评审,热力图在肺腺癌、乳腺浸润性癌、甲状腺癌等多种临床场景下,均展现出优秀的预测效果,并能有效规避血管、纤维组织及各类制片伪影的干扰。
更为关键的是,Soft MoE-ViT架构在追求强大性能的同时,打破了传统大模型对超高算力的过度依赖,将部署门槛降低到了普适化的临床级别。该模型经过推理效率优化,仅需24GB显存的显卡即可完成高效运行,实际显存占用甚至小于5GB。这意味着医疗机构在手术室周边即可实现全本地化的即时部署与即时反馈,这种轻量化且高能效的特性,为人工智能技术真正渗透到基层医院及资源受限地区的手术一线扫清了核心障碍,通过显著提升数智化病理诊断的可及性,实现了对生命健康的公平守护。
这一研究成果的发表,不仅是数智化病理在术中快速诊断场景下的里程碑式跨越,更是精准医疗理念从算法前沿向临床实践深度转化的生动诠释。透彻未来将持续深耕病理人工智能领域,致力于将复杂的病理图像转化为精准的决策支撑,让每一份病理切片都能成为守护生命的力量。


